Als spezifische Erstarrungswärme bezeichnet man die zum Erstarren einer Flüssigkeit abzuführende Wärmeenergie pro Kilogramm des Stoffes!
Schmelzen und Erstarren
Im Artikel zur spezifischen Schmelzwärme wurde ausführlich erläutert, dass beim Schmelzen eines Feststoffes Energie zum Aufbrechen der Bindungen nötig, damit der Stoff in den flüssigen Zustand überführt werden kann. Diese Energie wird dem Stoff in Form von Wärme zugeführt und wird Schmelzwärme genannt. Dabei bleibt bei Reinstoffen die Temperatur während des Schmelzens konstant.

Soll der flüssige Stoff wieder erstarren, dann muss diesem die zuvor zugeführte Wärme wieder entzogen, damit sich die Moleküle wieder stärker aneinander binden können. Die während der Erstarrung der Flüssigkeit zu entziehende Wärme wird in diesem Fall Erstarrungswärme genannt. Auch während des Abführens der Erstarrungswärme bleibt die Temperatur dabei konstant. Sie sinkt erst wieder, wenn der flüssige Stoff vollständig erstarrt ist. Der Temperaturpunkt, bei dem ein Stoff erstarrt, entspricht dem Schmelzpunkt des Stoffes (Erstarrungspunkt).
Eine detailliertere Erklärung für die Notwendigkeit der Wärmeabfuhr während des Erstarrens und der Grund weshalb dabei die Temperatur konstant bleibt findet sich im Artikel Warum bleibt die Temperatur bei einer Änderung des Aggregatzustandes konstant? wieder.
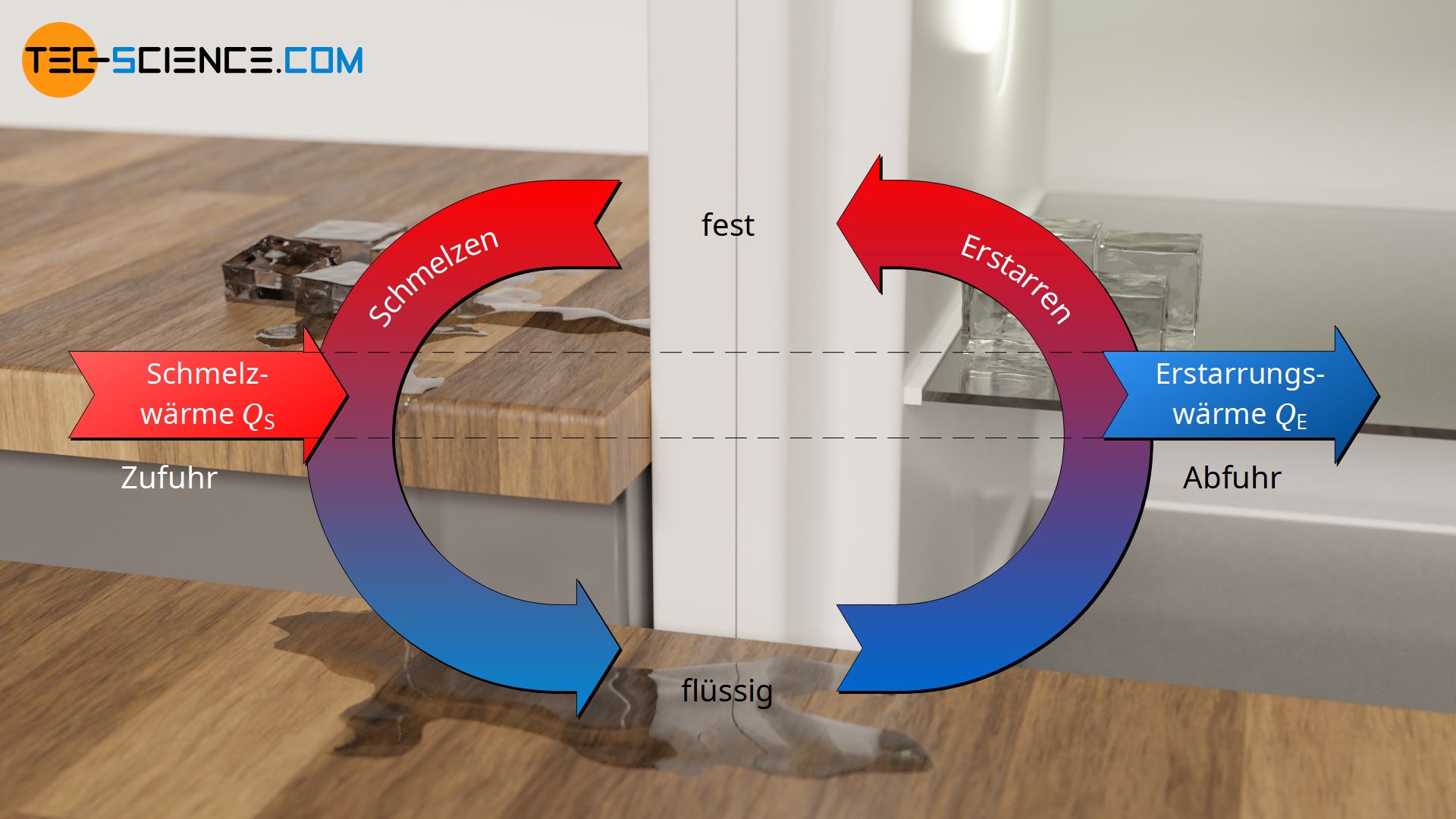
Spezifische Schmelzwärme und Erstarrungswärme
Aufgrund der Energieerhaltung entspricht der Wärmebetrag, der zum Schmelzen eines Stoffes zugeführt wurde (Schmelzwärme), jener Wärmemenge, die beim Erstarren wieder abgeführt werden muss (Erstarrungswärme). Aus diesem Grund ist auch die spezifische Erstarrungswärme qE, als Verhältnis von Erstarrungswärme QE und erstarrter Masse mE, genauso groß wie die spezifische Schmelzwärme qS.
\begin{align}
&\boxed{q_\text{E} = \frac{Q_\text{E}}{m_\text{E}}}~~~\text{mit}~~~\boxed{q_\text{E} = q_\text{S}} \\[5px]
\end{align}
Im Artikel Spezifische Schmelzwärme (latente Wärme) sind für ausgewählte Stoffe die spezifischen Schmelzwärmen bzw. Erstarrungswärmen aufgeführt. Anhand dieser Werte kann die abzuführende Erstarrungswärme QE in Abhängigkeit der zu erstarrenden Masse mE wie folgt ermittelt werden:
\begin{align}
&\boxed{Q_\text{E} = m_\text{E} \cdot q_\text{E}}\\[5px]
\end{align}
Auch man im Falle der Erstarrungswärme spricht man wieder von einer latenten Wärme, da sich die abzuführende Wärme beim Erstarren nicht direkt in einer Temperaturänderung niederschlägt (vom Lateinischen latere, was so viel bedeutet wie „verborgen sein“ oder „sich verstecken„).
Im Falle von Wasser ist die beim Erstarren abzuführende latente Wärme mit 334 kJ pro Kilogramm ungefähr so groß, wie jene Wärmemenge, die man bräuchte um das Wasser ausgehend von Raumtemperatur zum Kochen zu bringen. Es handelt sich also um sehr große Wärmemenge die abzuführen ist bzw. die vom flüssigen Wasser beim Erstarren abgegeben wird. Dies erklärt zum Beispiel warum das Beregnen von Pflanzen mit Wasser bei Temperaturen unterhalb des Gefrierpunktes als Frostschutz eingesetzt wird.






